Primero aclararemos que es una
mezcla, una mezcla es, la unión de dos o más elementos, o de un compuesto sin
que se combinen químicamente; es decir, las sustancias que se juntan no pierden
sus propiedades originales.
Separación de mezclas. Como las
sustancias extraídas de la naturaleza, que se obtienen en el laboratorio y en
la industria, están impurificadas con otras sustancias, la química emplea diversos
procedimientos para separar los componentes de dichas mezclas.
- DECANTACIÓN: se emplea para separar dos o más líquidos que no se disuelven entre sí, y que tienen diferentes densidades. También para separar las partículas de un solidos insolubles en un líquido, y que por su mayor densidad sedimentan, inclinando el recipiente de una mezcla y dejando escurrir el líquido en otro recipiente se logra la separación de los líquidos o de las partículas de solido sedimentado.
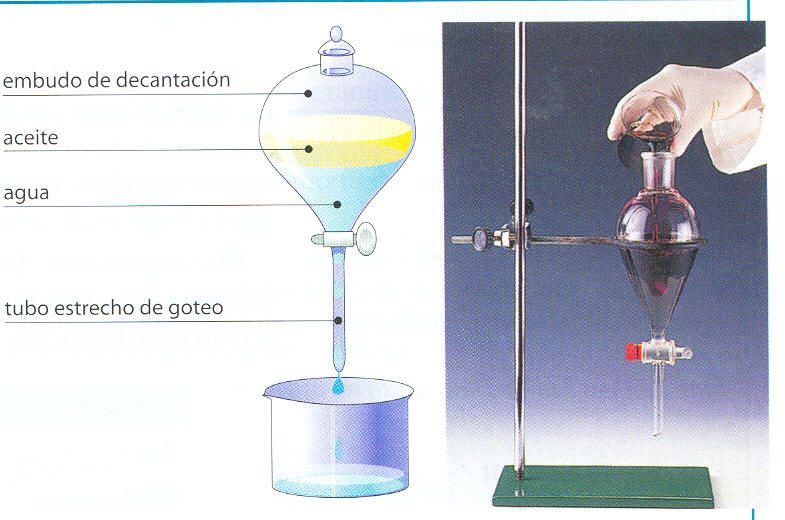 |
| DECANTACIÓN |
- CENTRIFUGACIÓN: cuando la sedimentación es muy lenta, se acelera mediante la acción de la fuerza centrífuga. Se pone una mezcla en un recipiente, el cual se hace girar a gran velocidad; la sustancia con mayor densidad queda en el fondo del recipiente y sobre ella la de menor densidad.
 |
| CENTRIFUGA DE LABORATORIO DENTAL |
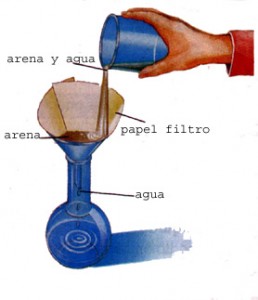
- FILTARCIÓN: separa las partículas sólidas insolubles que están en un líquido. Para efectuarla se utiliza un medio poroso que deja pasar el líquido y retiene las partículas de la sustancia sólida.
En el laboratorio se emplea el
papel filtro; en la industria se utilizan telas, fieltros lana de vidrio,
porcelana porosa etc.
- EVAPORACIÓN: se emplea para separar un sólido disuelto en un líquido. Cuando este se evapora la sustancia solida queda cristalizada. Los rayos solares evaporan el agua de mar y se obtiene la sal de cocina. En el laboratorio se pone en un vidrio de reloj una solución de yodo en éter: al volatilizarse este el yodo se cristaliza.
 |
| EVAPORACIÓN EN LABORATORIO |
- DESTILACIÓN: se utiliza para purificar un líquido, eliminándole las sustancias que tenga disueltas, o para separar mezclas de líquidos que se disuelven entre si con diferentes puntos de ebullición, es decir, que hierven a distinta temperatura. Consiste en producir mediante calor regulado, la vaporización del líquido y por enfriamiento su condensación.
En el laboratorio de hace la
destilación con un dispositivo formado principalmente por un matraz, un
termómetro y un condensador de liebig.
 |
| DESTILACIÓN EN EL LABORATORIO |
DESTILACIÓN FRACCIONADA: se
emplea en las refinerías para separar del petróleo crudo sus diversos
componentes: gas natural, gasolina, keroseno, gas, oil etc. Aprovechando que cada
uno de ellos tiene diferente punto de ebullición.
- SUBLIMACIÓN: es el paso directo de un cuerpo en estado sólido al gaseoso sin pasar por la fase liquida. Este se aprovecha para separar una mezcla de partículas de dos sustancias sólidas, cuando una de ellas puede sufrir sublimación. Ejemplo cristales de yodo mezclado con polvo de carbón.
- DISTINTA SOLUBILIDAD: se emplea para separar la mezcla de dos sustancias cuando una de ellas es soluble en determinado líquido. Por ejemplo: una mezcla de azufre y polvo de fierro se separa agregándole disulfuro de carbono; éste se disuelve únicamente el azufre. Filtrado con el papel filtro, en el que queda el polvo de fierro. El azufre disuelto en el disulfuro de carbono se recoge en un vidrio de reloj; al evaporarse el disulfuro de carbono, el azufre quedara cristalizado.


No hay comentarios:
Publicar un comentario